Bíró Szabolcs állításából ezt szűrheti le az olvasó:
A B1-vitamin legjobb formája a tiamin-pirofoszfát (=tiamin-difoszfát, TPP). A szabad tiamin források (tiamin-HCl és tiamin-monotitrát) kevésbé jók, ezért olyan készítményt érdemes keresni, amikben a B1-vitamin tiamin-pirofoszfát (TPP) formában van jelen.
Bíró Szabolcs indoklása:
Mivel a sejteken belül a TPP az aktív koenzim forma, ami a tiaminból keletkezik bennük, ezért szerinte eleve szedjük azt, mert a sima tiamin inaktív. Semmiféle indoklást nem ad azzal kapcsolatban, hogy miért következik ebből, hogy a TPP szájon át történő szedése lenne a jobb forma. Egyszerűen csak egymás után többször ezt állítja, hogy az jobb és azt kell szedni, majd kiemelve nagy betűkkel, bekeretezve is. Semmilyen referenciát nem ad meg, hogy mindezt mire alapozza, csak a sok ismétléssel igyekszik ezt az olvasó fejébe sulykolni.
Az én állításom:
Pont az ellenkezője. A B1-vitamin legjobb formája a sima mezei tiamin (tiamin-hidroklorid és tiamin-mononitrát), míg a Szabolcs által ajánlott, sejten belüli aktív koenzim forma, a TPP (a TMP-vel és TTP-vel egyetemben) a legkevésbé jó forma, annak ugyanis előbb sima tiaminra kell bomlania enzimatikusan, hogy egyáltalán föl tudjon szívódni. A legjobb esetben (elegendő emésztő- és egyéb enzim termelődése esetén) azonosan jó csak, mint a szabad tiamin, rosszabb esetben (ha nincs elég enzim) még csak nem is hasznosul a szájon át szedett TPP.
Az én indoklásom:
(referenciák a végén)
Szabolcs arról feledkezhetett meg az ajánlásakor, hogy az étrend-kiegészítőket emésztőrendszerrel, vérrel és enzimekkel rendelkező emberek szedik be, nem pedig a sejtjeink kapkodják be őket. Minden, amit Szabolcs leír a TPP előnyeiről, az a sejtekbe már bejutott TPP-ről szól, csakhogy sima tiamin formájában a B1 sokkal inkább eljut a sejtekhez TTP-ként, mint a szájon át szedett TTP.
No, de haladjunk sorban és nézzük meg, hogy milyen formában fordul elő a B1 az élelmiszerekben és étrend-kiegészítőkben, majd nézzük meg, hogy mi történik a különböző elfogyasztott B1-formákkal és hogyan jutnak el a sejtjeinkhez.
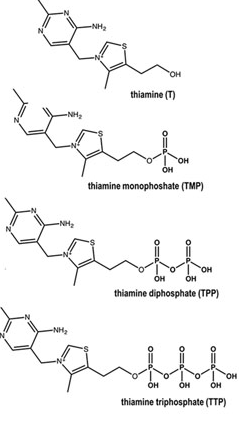
A B1-vitamin élelmiszerekben és szervezetünkben is előforduló formái a tiamin (szabad tiamin) és annak foszfoészterei, a tiamin-monofoszfát (TMP), a tiamin-difoszfát vagy másik nevét tiamin-pirofoszfát (TPP) és a tiamin-trifoszfát (TTP). Állati eredetű élelmiszerekben a tiamin-foszfoészterek dominálnak, főleg a TTP, míg növényi élelmiszerekben inkább a szabad tiamin fordul elő.
Étrend-kiegészítőkben is ezek fordulnak elő, pontosabban ezek sói, tehát a szabad tiamin tiamin-hidroklorid és tiamin-mononitrát formában, míg a TMP és TPP (TTP nincs) TMP- és TPP-klorid formájában.
Mi történik miután lenyeltük őket?
Élelmiszerekben a szabad tiamin és tiamin-foszfoészterek az élelem fehérjéihez való kötésből fölszabadulnak az emésztés során, majd szabad tiamin, illetve TMP, TPP és főleg TTP formában lesznek jelen a vékonybelünkben, ahol a különböző enzimek mindet szabad tiaminra bontják.
A kiegészítőkből szedett B1 esetében még egyszerűbb a helyzet. Itt nem kell a fehérjékhez kötött állapotukból felszabadulniuk, mert ahogy minden só bármilyen folyadékban szétesik ionjaira, így ezek is. Lenyelést követően a gyomrunkban a tiamin-hidroklorid azonnal szabad tiaminná és sósavvá alakul (disszociál), a tiamin-mononitrát szabad tiaminná és nitráttá, míg a TMP- és TPP-klorid TMP/TPP-vé és kloriddá.
A TMP és TPP nem képes hasznosulni, csak miután szabad tiaminná alakult. Különböző nem specifikus enzimek végzik ezt a szabad tiaminná alakítást (az észter kötés felbontását), főleg az alkaikus foszfatáz nevű enzim, amely a vékonybelünkben és sok egyéb szövetünkben, valamint a vérünkben is megtalálható.
Bármilyen formában is jutottunk tehát B1-hez, a vékonybelünkben mind szabad tiaminná alakul. Ha valami egy enzim hiányában nem tudna 100%-osan átalakulni, akkor hasznosulni sem tud a TMP vagy TPP, így tovább jut a vastagbélbe, ahol a baktériumok martalékává válik. Amennyiben elég magas a dózis, talán eljuthat a vastagbél egy speciális területére, ahol a vastagbél sejtjei képesek lehetnek a TPP-t felvenni, bár ezesetben sem kerül be a szisztémás keringésbe, csupán a vastagbél sejtjeinek szolgál tápanyagul.
Hogyan jut el a B1-vitamin a sejtjeinkhez és eleve a véráramunkba?
A vékonybelünkön keresztül történik a szisztémás keringésbe való bejutása a B1-nek, amihez előbb szabad tiamin formává kell alakulnia abban az esetben, ha nem olyan formában jutottunk hozzá. Ez a szabad tiamin a vékonybelünk sejtjeiben részben TPP-vé alakul, majd – mivel a TPP nem képes kijutni a vékonybél sejtjeiből, ahhoz hogy a véráramba jusson – átalakul TMP-vé. A vékonybelünkből tehát csak szabad tiamin és TMP jut a véráramunkba, és kizárólag ezek tudnak eljutni a sejtjeinkhez. A sejtjeink a szabad tiamint fel tudják venni, míg a TMP-t előtte nekik is szabad tiaminná kell alakítaniuk, hogy hozzájussanak. A TMP és tiamin egyaránt a sejtbe való bejutás során, és a sejtben is TPP-vé, TTP-vé és TMP-vé alakul. A TPP a legfontosabb, ő a koenzim forma a sejteken belül. A vérünkben nincs szabadon keringő TPP, csak tiamin és TMP. TPP csak sejteken belül (intracellulárisan) található meg.
Összességében tehát láthatjuk, nem elég, hogy a vékonybelünk is csak a szabad tiamint tudja felvenni és továbbjuttatni a vérbe (részben TMP-vé alakított formájában), de a sejtjeink is csak a szabad tiamint tudják felvenni. A kész, aktív koenzim formája a B1-nek (TPP) tehát a sejtjeinkben állítódik elő, ebben a formában történő bevétele előnnyel nem tud járni, de hátránnyal igen!
Miért hátrányos a B1-et a már sejten belül aktív formájában szedni, azaz tiamin-pirofoszfát (TTP) formájában?
Ahogy már volt róla szó, hasznosítás előtt enzimeknek kell átalakítani a TTP-t szabad tiaminná, azaz egy lépéssel többet igényel a szervezetünktől. Miután átalakult sima tiaminná, utána már ugyanaz történik vele, mintha sima tiamint szedtünk volna be. Értelemszerűen, ha nincs elég emésztőenzimünk a vékonybelünkben, főleg ha az alkaikus foszfatáz szintünk nem elegendő, akkor feltételezhető, hogy nem megy végbe az átalakulás, mely esetben az át nem alakult rész képtelen hasznosulni, legalábbis szisztémásan biztosan nem. Legjobb esetben (és ez is nagyon esetleges) a vastagbelünk sejtjei számára szolgáltathat némi muníciót, amennyiben a bélbaktériumok addig nem élik fel. Magnéziumhiány esetén, illetve fogamzásgátló szedés esetén, ahogy cukorbetegség, ischémiás szív/ér-betegség, magas kortizol szint vagy pajzsmirigy-alulműködés esetén is gyakran az alkaikus-foszfatáz mennyiség elégtelen, de gyulladásos bélproblémák esetén is kompromittált az emésztőenzimek mennyisége. Ilyen esetekben fennáll a kockázata, hogy megfelelően csak a tiamin-hidroklorid és -mononitrát forma tud hasznosulni, hiszen azok eleve szabad-tiamint szolgáltatnak, nem kell már átalakítani.
A másik probléma, hogy a TPP felszívódása feltehetően eleve rosszabb még egészséges, foszfatáz enzimekben bővelkedő embereknél is, mint a sima tiaminé, legalábbis megfelelően magas bevitel esetén. Miért? A sima (szabad) tiamin felszívódása bár nem rossz, a bevett mennyiség (bélben lévő koncentráció) növekedésével a felszívódás szinte tökéletessé válik, ugyanis nagy bélkoncentráció esetén passzív transzporttal is felszívódik, míg kisebb koncentrációban csak különböző (kisebb hatékonyságú) aktív transzportfehérjék segítségével tud. Amennyiben viszont nem kész tiaminhoz jutunk hozzá, hanem annak tévesen bioaktívabbnak nevezett foszfoésztereihez (pl TPP), azoknak előbb ugye szabaddá kell válniuk, mely enzimatikus átalakulás elnyújtottá teszi a szabad tiamin megjelenését a belekben, azaz nem tud akkora bélkoncentráció létrejönni, mintha eleve sima tiamint nyeltünk volna le.
Mindösszesen egyetlen vizsgálat létezik, ahol a B1 különböző formáit összehasonlították, ezt is sertéseken végezték. Olyan növényi élelmiszereket adtak nekik, amelyek főként tiamint tartalmaznak, illetve olyanokat, amelyek főleg a foszfát formáikat. Nagyjából azonos hasznosulása volt mindnek: A sima tiaminban bővelkedő élelmiszerekből 77-94%-os, míg a B1 „aktív” foszfát formáiban bővelkedő élelmiszerekből hajszálnyit rosszabb, 73-88% közötti hasznosulást figyeltek meg. (Roth-Maier et al., 1999. Investigations on the intestinal availability of native thiamin in selected foods and feedstuffs. Eur. J. Nutr. 38, 241-246.)
Milyen problémát okozhat a fogyasztó számára TPP-t tartalmazó termékek fogyasztása?
- Különböző egészségügyi állapotok esetén (gyulladásos bélproblémák, pajzsmirigy-alulműködés, cukorbetegség, szív/érrendszeri betegségek, Zn/Mg hiány, fogamzásgátlók szedése, Wilson-kór, anémia, magas kortizol, stb) a TPP hasznosulásához (sima tiaminná alakulásához) szükséges enzimek szintje alacsony, így pont, akiknek szánják az aktívnak hitt B1 formákat, azok számára lesz hatástalan vagy legalábbis biztosan kevésbé hatásos, mint a sima tiamin.
- A TPP drágább, mint a tiamin, miközben a legjobb esetben is csak azonos hatású -> kidobott pénz
- Amennyiben a termék fejlesztője tévesen úgy véli, hogy a TPP egy bioaktívabb forma és emiatt kevesebbet tesz a termékbe, akkor valójában csak túl kevés B1-et tett bele, miközben maga is és a fogyasztó is abban az illúzióban van, hogy bőséges B1-et szed, miközben túl keveset.
- Ha valaki nagy dózisban szeretne B1-et szedni, mert attól vár állapotváltozást, akkor még egészséges emberek esetében is el fog maradni a hasznosulás a sima tiaminhoz képest -> elmaradhat a hatás, ami rossz következtetéshez vezeti a fogyasztót és a kezelőjét is (például, hogy nem is használ az állapotának a nagyobb dózis B1, holott használna, csak nem az aktívnak hitt formával kellene próbálkoznia.)
Megoldási javaslat az elfogyasztott TPP közvetlen sejtbe juttatására:
Mivel az elfogyasztott TPP sima tiaminná alakulás nélkül sehogyan sem képes eljutni a vérünkbe sem, nemhogy a sejtjeinkbe, ezért az egyetlen lehetőség az, ha közvetlenül a sejtjeinkbe injekcióznánk a TPP-t (a vérbe nem elég). Ez nyilván kivitelezhetetlen. Azonban, ha a TPP-t nanokolloid rendszer részeként juttatjuk magunkba, pl ún. unilamelláris, 200nm körüli vagy kisebb liposzómákba, nioszómákba vagy hasonlókba zárva, akkor akár szájon át fogyasztva is intakt formában maradnak, és jutnak be a sejtekbe, eljuttatva így a TPP-t a célterületére, a sejteken belülre. Így egyáltalán nem kell átalakítanunk, majd vissza. Mindez meglehetősen fölösleges is volna, hiszen nem ismert olyan állapot, ahol a sima tiamin ne tudna megfelelően TPP-vé alakulni. Kivétel a Mg hiánya, így egyszerűen csak arról kell gondoskodnunk, hogy ne legyünk Mg hiányosak. Bárhogy is, a TPP csak nanokolloid rendszer részeként jelenthet előnyt a sima mezei tiaminhoz képest, minden egyéb esetben csak hátrányt jelent.
Összefoglalva:
A B1-vitamin bármilyen formáját is nyeljük le, az a beleinkben már mind sima tiamin formára fog alakulni, hisz anélkül felszívódni sem tudna, majd a véráramunkba érve a sejtjeink is csak a sima mezei tiamint képesek felvenni. A B1-vitamin sejten belül aktív koenzim formáját (TPP) orálisan szedni tehát a legjobb esetben is kidobott pénz, rosszabb esetben meg akár nem is ér semmit. Amiért Szabolcs a B1 TPP formáját ajánlja, az azért lehet, mert elfeledkezett róla, hogy az étrend-kiegészítőket nem a sejtjeink szedik be, hanem emberek, akikben a TPP csak akkor tud eljutni a sejtekhez, ha az előbb sima tiaminra bomlott. A TPP orális szedése tehát egy lépéssel távolabb van a sejten belüli TPP létrejöttében, mint a sima tiamin orális szedése, nem pedig előrébb, mint Szabolcs hiszi. A sejtben valóban előrébb van több lépéssel, de ahhoz azt a sejtbe kéne injekciózni vagy a már fentebb említett nanokolloid…
Felhasznált szakirodalom
(A bennük lévő releváns szöveget is mutatjuk, akit érdekel és nem szeretné végig bogarászni őket)
1. Dhir, Shibani et al. “Neurological, Psychiatric, and Biochemical Aspects of Thiamine Deficiency in Children and Adults.” Frontiers in psychiatry vol. 10 207. 4 Apr. 2019, doi:10.3389/fpsyt.2019.00207
Link: https://www.frontiersin.org/articles/10.3389/fpsyt.2019.00207/full
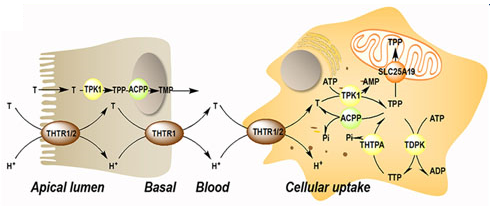
Dietary thiamine is mainly in the form of phosphate derivatives and, before absorption, these are converted to free thiamine by intestinal phosphatases. Mammalians utilize THTR1 and THTR2 to transport thiamine. The THTR1 appears to function in the micromolar range, whereas the THTR-2 appears to function in the nanomolar range. Both transporters are expressed in the human small and large intestine, and the expression of THTR1 is higher than that of THTR2, with THTR1 found at both the apical and basolateral membranes of enterocytes (somewhat higher expression at the latter compared to the former domain). Expression of the THTR2 protein was found to be restricted to the apical membrane domain only [see (5) and references therein]. Free thiamine is converted to TPP by the action of TPK1 in the cytosol and dephosphorylation of TPP to TMP and thiamine by ACPP. At higher concentrations of thiamine, simple passive diffusion takes place [see (6) and references therein]. From blood, thiamine is taken up by either transporter (THTR1 or THTR2). Both carriers are widely distributed in the body, but the levels differ in different tissues. Once inside the target cells, thiamine is phosphorylated to TPP by TPK1 and to TTP by TDPK. Both TPP and TTP can be dephosphorylated by ACPP and THTPA, respectively.
Dietary Availability, Absorption, and Cellular Uptake
As with most hydrophilic micronutrients, thiamine absorption occurs mainly in the jejunum (33). Throughout the digestive tract, dietary proteins get hydrolyzed, releasing thiamine. In the intestinal lumen, alkaline phosphatases catalyze the hydrolysis of thiamine-phosphorylated derivatives into free thiamine (34). Unphosphorylated, free thiamine at concentrations higher than 1 µM enters the enterocyte by passive diffusion, whereas at lower levels, it is transported via the saturable thiamine/H+ antiport system (thiamine transporter 1 or THTR1) through an energy-dependent process (33). Under conditions of thiamine deficiency, an upregulation of the expression of the thiamine transporter 2 (THTR2) was observed in Caco2 cells in culture, suggesting that diet can modulate the expression of this transporter (35). Within the enterocyte, thiamine is phosphorylated to thiamine pyrophosphate (TPP) by TPK1. Then, most TPP is dephosphorylated to thiamine monophosphate (TMP) to cross the basal membrane of the enterocyte. The TMP is released into the bloodstream through an ATPase-dependent transport system (36) (Figure 1B). Free thiamine can also reach the bloodstream via the thiamine transporter 2 (THTR2) located mainly at the basolateral membrane of the enterocyte. Once in blood, while very low levels of TMP and thiamine circulate free in plasma or serum, more than 90% of the phosphorylated thiamine (in the form of TPP) is present in erythrocytes and leukocytes (37). Notably, the isoform 3 of the carrier SLC44A4 has recently been described as a TPP carrier in the colon. Originally, SLC44A4 was described as a choline transporter linked to the non-neuronal synthesis of choline (38) and required to the efferent innervation of hair cells in the olivocochlear bundle for the maintenance of physiological function of outer hair cells and the protection of hair cells from acoustic injury (39). Recent evidence indicates that this carrier may mediate the absorption of microbiota-generated TPP (especially in infants) and contribute to host thiamine homeostasis (40).
The cellular uptake of thiamine from the bloodstream can be mediated by any of the two high-affinity carriers: THTR1 [encoded by SLC19A2 (41)] and THTR2 [encoded by SLC19A3 (42, 43)]. These transporters are ubiquitously expressed (42–44), but THTR1 is most abundant in the intestine, skeletal muscle, nervous system, and eye followed by the placenta, liver, and kidney, whereas THTR2 is located mostly in adipose tissue, breast tissue, liver, lymphocytes, spleen, gallbladder, placenta, pancreas, and brain (information collected from GeneCards). Once transported intracellularly, free thiamine is rapidly phosphorylated to TPP by thiamine pyrophosphokinase (TPK1). A second kinase, TDPK, adds a phosphate group to TPP to generate thiamine triphosphate (TTP). TPP and TTP can be dephosphorylated to, respectively, TMP and TPP by phosphatases [Prostatic Acid Phosphatase (ACPP) and THTPA, respectively; Figure 1B].
2. Yoshii, Ken et al. “Metabolism of Dietary and Microbial Vitamin B Family in the Regulation of Host Immunity.” Frontiers in nutrition vol. 6 48. 17 Apr. 2019, doi:10.3389/fnut.2019.00048
Dietary TPP is hydrolyzed by alkaline phosphatase and converted to free thiamine in the small intestine (22). Free thiamine is absorbed by the intestinal epithelium via thiamine transporters (e.g., THTR-1, THTR-2) and transported to the blood for distribution throughout the body (11). Free thiamine is converted back to TPP and is used for energy metabolism in the TCA cycle.
3. Scientific Opinion of the Panel on Food Additives and Nutrient Sources added to Food (ANS)
Link: https://efsa.onlinelibrary.wiley.com/doi/pdfdirect/10.2903/j.efsa.2008.864
Thiamine can be esterified at the hydroxyethyl side chain. The most important esters are thiamine monophosphate, thiamine pyrophosphate and thiamine triphosphate (SCF, 2001). In most animal products 95-98% of thiamine occurs in a phosphorylated form, with about 80- 85% as thiamine triphosphate. In plants thiamine occurs in the non-phosphorylated form (Gubler, 1991; Gregory, 1997). Thiamine occurs in the human body as free thiamine and its phosphorylated forms: thiamine monophosphate, thiamine triphosphate, and thiamine pyrophosphate, of which the latter is also known as thiamine diphosphate or cocarboxylase. Thiamine occurs in cells principally in its active coenzyme form called thiamine pyrophosphate (cocarboxylase).
Thiamine pyrophosphate chloride is the diphosphate form of thiamine (vitamin B1) and this form occurs in foods in vegetables, cereals, legumes, meats, yeast and E. coli (Golda et al., 2004; Watanabe et al., 2004; Machlin, 1984).
After a normal meal, thiamine is mainly in the free form in the intestinal lumen, since its phosphoesters have probably been completely hydrolysed by different phosphatases of the gastrointestinal tract (Rindi and Laforenza, 2000).
Whereas thiamine pyrophosphate exists intracellularly exclusively, thiamine and thiamine monophosphate are present both intracellularly and extracellularly.
Once transported into the cells, thiamine monophosphate may be converted to thiamine by thiamine monophosphatase, followed by phosphorylation to thiamine pyrophosphate by thiamine pyrophosphokinase. Thiamine pyrophosphate is the physiologically active form of thiamine that acts as coenzyme in the decarboxylation of α-ketoacids and in transketolase reactions (Gubler, 1991).
The metabolic fate of thiamine was reviewed by the Expert Group on Vitamins and Minerals (EVM, 2002). The EVM stated that prior to absorption phosphorylated forms of thiamine undergo complete hydrolysis involving a number of intestinal phosphatases, and that consequently thiamine found in the intestinal lumen following a meal is in the free form (EVM, 2002; Haas, 1988).
Csökkent alkaikus foszfatáz enzim szintel járó állapotokkal kapcsolatos referenciák:
- https://pubmed.ncbi.nlm.nih.gov/7720239/
- https://www.hindawi.com/journals/dm/2019/8473565/
- https://www.foodandnutritionjournal.org/volume5number3/low-alkaline-phosphatase-alp-in-adult-population-an-indicator-of-zinc-zn-and-magnesium-mg-deficiency/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2882585/
- https://pubmed.ncbi.nlm.nih.gov/4003329/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4881751/
- https://www.nature.com/articles/2071292b0
- https://journals.asm.org/doi/10.1128/IAI.02520-14
- https://pubmed.ncbi.nlm.nih.gov/9877094/
- https://pubmed.ncbi.nlm.nih.gov/16010458/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4062654/
